Inoserp PAN-AFRICA
C'est une préparation stérile, hautement purifiée et lyophilisée, de fragments équins d'immunoglobuline F(ab´)2 neutralisant les venins avec une haute spécificité.
Région
Cést un antivenin polyhvalent dórigine équine spécifiquement indiqué pour le traitement des envenimations après morsures de serpents d'Afrique sub-Saharienne.
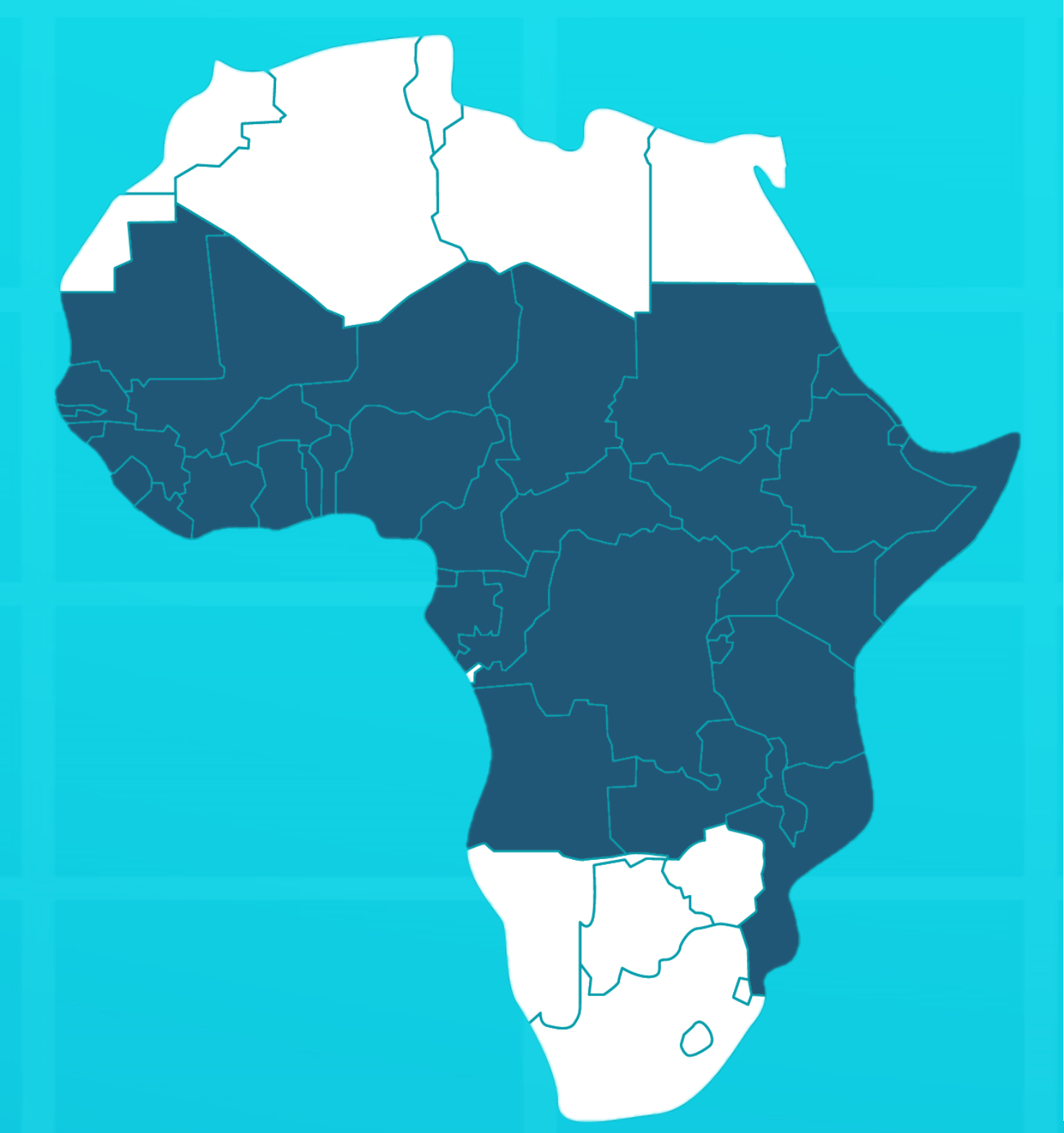
Espèces
- Viperidae:
- Bitis arietans, Bitis gabonica, Bitis nasicornis, Bitis rhinoceros, Echis leucogaster, Echis ocellatus, Echis pyramidum.
- Elipidae:
- Dendroaspis angusticeps, Dendroaspis jamesoni, Dendroaspis polylepis, Dendroaspis viridis, Naja haje, Naja katiensis, Naja melanoleuca, Naja nigricollis, Naja nubiae, Naja pallida, Naja senegalensis.
QUESTIONS MEDICALES FREQUENTES & REPONSES
- Quelle est la composition d’InoserpTM PAN-AFRICA?
InoserpTM PAN-AFRICA est composé d’anticorps ciblant spécifiquement les espèces les plus dangereuses d’Afrique sub-Saharienne. InoserpTM PAN-AFRICA est un antivenin polyvalent car il couvre plusieurs espèces.
En savoir plus
InoserpTM PAN-AFRICA est composé d’anticorps d’origine équine ou fragments d’immunoglobuline F(ab’)2, qui ont été conçus pour neutraliser les venins des espèces médicalement importantes de la région sub-Saharienne.
-
Quelles sont les espèces couvertes par InoserpTM PAN-AFRICA?
InoserpTM PAN-AFRICA couvre les envenimations des espèces de serpent les plus dangereuses d’Afrique sub-Saharienne. Au total, 18 espèces médicalement importantes sont couvertes, à la fois vipéridés et élapidés, comme suit:
Viperidae: Bitis arietans, Bitis gabonica, Bitis nasicornis, Bitis rhinoceros, Echis leucogaster, Echis ocellatus, Echis pyramidum.
Elapidae: Dendroaspis angusticeps, Dendroaspis jamesoni, Dendroaspis polylepis, Dendroaspis viridis, Naja haje, Naja katiensis, Naja melanoleuca, Naja nigricollis, Naja nubiae, Naja pallida, Naja senegalensis.
En savoir plus
Une étude récente a montré que l’antivenin couvrait en réalité 6 espèces additionnelles par cross-neutralisation: Atractaspis irregularis, Cerastes cerastes, Dispolidus typus, Naja anchieta, Naja annulifera, Naja mossambica. En tout, avec 24 espèces, InoserpTM PAN-AFRICA offre la protection la plus large contre les espèces médicalement importantes en Afrique sub-Saharienne.(1)
-
Quelles sont les spécificités des antivenins d’Inosan Biopharma antivenoms?
Le antivenins d’Inosan Biopharma ont été conçus pour offrir la meilleure protection contre la plupart des espèces médicalement importantes tout en garantissant la plus grande sécurité d’utilisation, ce grâce à la qualité élevée du processus de fabrication
En savoir plus
- Les antivenins d’Inosan Biopharma sont polyvalents et couvrent la plupart des espèces médicalement importantes d’une région donnée. Les venins utilisés pour le processus d’immunisation proviennent d’espèces représentatives des régions pour lesquelles les antivenins sont destinés.
- Les antivenins d’Inosan Biopharma sont composés de fragments d’immunoglobuline F(ab’)2 hautement spécifiques(2), ce qui signifie qu’il y a une proportion élevée de F(ab’)2 efficaces, capables de se lier spécifiquement aux composants toxiques des venins et de les neutraliser. Grâce à cette haute spécificité, les antivenins d’Inosan Biopharma peuvent inclure un plus grand nombre d’espèces dans un même flacon, tout en ayant un taux de protéines peu élevé.
- Les antivenins d’Inosan Biopharma sont hautement purifiés avec un taux de F(ab’)2 atteignant 95%(2). Ils ont un faible taux de protéines (<10%, pas plus de 100 mg of protéines par mL dans le produit reconstitué) et sont sans conservateurs.
-
Quel est le profil d’efficacité d’InoserpTM PAN-AFRICA?
InoserpTM PAN-AFRICA bénéficie de l’évaluation clinique la plus large en Afrique sub-Saharienne en comparaison des autres antivenins. Toutes les études réalisées ont montré qu’InoserpTM PAN-AFRICA réduit rapidement les saignements et les troubles neurotoxiques.(3).
En savoir plus
Il a été montré que le taux d’amputation et de décès était très bas suite à l’utilisation d’InoserpTM PAN-AFRICADans une revue indépendante récente sur les données cliniques disponibles, InoserpTM PAN-AFRICA apparaît ayant le rapport bénéfice/risque le plus favorable parmi les antivenins polyvalents disponibles en Afrique sub-Saharienne(4).
-
Quel est le profil de tolérance d’InoserpTM PAN-AFRICA?
L’utilisation à grande échelle de l’antivenin ainsi que les études cliniques conduites jusque-là, ont montré qu’InoserpTM PAN-AFRICA est très bien toléré. Lorsqu’ils surviennent, les effets indésirables sont généralement d’intensité légère et disparaissent spontanément ou
En savoir plus
D’après les études cliniques réalisées, les effets indésirables ont été rapportés idans moins de 10% des patients<(5). Ils peuvent inclure des transpirations, nausées, éruptions cutanées, baisse modérée de la pression sanguine, réaction anaphylactoïde (de type allergique) associée avec un érythème facial et une toux. Le risque de choc anaphylactique ne peut être exclu mais reste très rare. Des réactions similaires à la maladie sérique peuvent apparaître environ 6 jours après le début du traitement. Les signes cliniques sont fièvre, prurit, érythème ou urticaire, adénopathie et arthralgie. Cependant, ce type de réactions est observé dans moins de 1% des patients.
-
Quelles sont les recommandations pour l’administration d’InoserpTM PAN-AFRICA?
InoserpTM PAN-AFRICA doit être administré le plus tôt possible après les premiers signes d’envenimation afin d’obtenir l’efficacité maximale. La dose recommandée est de 2 flacons (voie IV). Un renouvellement du traitement (2 flacons) peut s’avérer nécessaire.
En savoir plus
InoserpTM PAN-AFRICA doit être administré par voie intra-veineuse en injection directe lente ou perfusion. Il est recommandé d’évaluer le patient toutes les 2 heures après l’administration initiale et de renouveler l’administration (2 flacons) aussi longtemps que les symptômes persistent ou s’aggravent Un plus grand nombre de flacons peuvent être administrés selon la sévérité ou le type d’envenimation comme les morsures neurotoxiques.
-
Existe-t-il des contre-indications à l’utilisation d’InoserpTM PAN-AFRICA?
L’antivenin ne doit pas être administré chez les personnes allergiques aux protéines d’origine équine ou aux excipients contenus dans le produit.
En savoir plus
Compte tenu du risque létal associé à l’envenimation, les antivenins d’Inosan Biopharma peuvent toutefois être administrés dans cette population spécifique (de patients allergiques aux protéines d’origine équine) à la condition qu’un éventuel choc anaphylactique puisse être prise en charge immédiatement.
-
A Y a-t-il des recommandations spécifiques pour l’utilisation d’InoserpInoserpTM PAN-AFRICA chez l’enfant?
La posologie doit être la même chez l’adulte et l’enfant, quel que soit le poids, car c’est la quantité de venin qu’il faut neutraliser.
En savoir plus
L’envenimation chez l’enfant conduit généralement à des symptômes plus sévères et à un taux plus élevé de létalité et de séquelles. Ceci est lié à leur masse et volume corporels plus petits entraînant une dilution moins grande du venin. Les données cliniques disponibles montrent que les profils de tolérance et d’efficacité dans la population pédiatrique ne sont pas différents de ceux chez l’adulte.(4).
-
Quelles sont les instructions pour le stockage d’InoserpTM PAN-AFRICA?
Les antivenins d’Inosan Biopharma sont lyophilisés, ils peuvent donc être conservés à température ambiante jusqu’à 30°C avec des écarts jusqu’à 40°C pour des périodes de temps réduites.
En savoir plus
Les antivenins d’Inosan Biopharma sont lyophilisés, ce qui rend leur utilisation très facile et peu couteuse en comparaison des présentations liquides, particulièrement dans les régions tropicales.
-
Le processus de fabrication d’InoserpTM PAN-AFRICA a-t’il la certification BPF?
Le processus de fabrication des antivenins d’Inosan Biopharma est en conformité avec les normes BPF les plus élevées en particulier concernant la reproductibilité des lots et la stabilité du produit..
En savoir plus
Inosan Biopharma maintient toutes les certifications BPF délivrées par la COFEPRIS, l’Agence Mexicaine, reconnue par l’OMS pour la qualification des fabriquants de vaccins et de produits biologiques. De plus, Inosan Biopharma suit le guidelines mis en place par l’OMS pour la fabrication des antivenins.
Pour plus d’information, merci de contacter: medinfo@inosanbiopharma.com
References...
<(1) Martinez et Al. Preclinical evaluation of the polyspecific antivenom InoserpTM PAN-AFRICA against the venoms of elapids and viperids of sub-Saharan Africa region: neutralization of toxic activities. World congress of IST 2019.
(2) Mathé et Al. A new generation of F(ab’)2 antivenoms made of highly purified and specific immunoglobulin fragments. Venoms Toxins 2020.
(3) Chippaux et Al. Snakebites in Cameroon: Evaluation of snake antivenom in Africa (ESAA) and real life conditions. Venom Week 2022.
(4) Potet et Al. Reviewing evidence of the clinical effectiveness of commercially available antivenoms in sub-Saharan Africa identifies the need for a multi-centre, multi-antivenom clinical trial. PLOS NTD 2019.
(5) Chippaux et Al. Evaluation of a new polyvalent antivenom against snakebite envenomation (Inoserp® Panafricain) in two different epidemiological settings: Northern Benin and Maritime Guinea]. Médecine et Santé Tropicales 2015.
